 南充艺术生培训文化课哪个学校好
南充艺术生培训文化课哪个学校好 【新学高考艺考生文化课补习班教学计划】
1.回归教材,注重基础,对知识进行全方位的、系统的复习,解决学生的基础知识问题。
2让学生重视知识的积累,学会构建自己知识体系。
3.老师开始精确讲解知识重点以及难点,同时训练学生对知识的掌握、做题的技能、学习的方法。
4.对之前复习的知识进行查漏补缺,过程中再巩固完善。
5.对专题专点加强训练,着重帮助学生渗透、贯通、运用各个知识点。
【新学高考师资介绍】
专业一线高考教研团队亲自授课,专属两名班主任24小时跟踪管理学员学习效果,及时调整学员的学习心态
 南充艺术生培训文化课哪个学校好
南充艺术生培训文化课哪个学校好 高三零诊考了410分,很沮丧,然后我同学让我去新学试试,他在哪里一直学还学得不错,我就想去试试。一个学期的时间,我的成绩就涨到了500多,老师说我还可以再进步,我很开心啊,真的是很棒的老师,学校环境也挺不错的,班主任很对我们很关心。很感谢新学的老师们,让我有了学习的兴趣,我会好好学习,天天向上!!
第一次来到新学高考总体感觉很好,校区干干净净的,教室、宿舍也宽阔明亮,接待咨询的老师也很热情,耐心的解答了我很多问题,给孩子测评后推荐了孩子适合的班型,师资方面也很优秀。
孩子已经在新学培训大半年年了,很感谢这里的老师,谈谈个人感受,课程安排比较合理,也会和家长沟通安排,老师对教学是很负责的,针对孩子的不足之处有针对性的教学,能及时发现孩子的问题,希望能给大家解决孩子的问题,祝越办越好。
 南充艺术生培训文化课哪个学校好
南充艺术生培训文化课哪个学校好 1、NA表示阿伏加德罗常数的值。下列判断中,正确的是
A.H2O2溶液中加入MnO2可制得O2,产生2.24L(标况)O2,转移0.4NA个电子
B.SO2和CO2都属于酸性氧化物,Na2O和A12O3都属于碱性氧化物
C.在氯化铵水溶液中,既存在水解平衡,又存在电离平衡
D.O2在放电的条件下生成O3属于化学变化,电解质溶液导电属于物理变化
【知识点】物质的量单元测试
【答案】
【答案】C
【解析】
试题分析:A、标准状况下2.24L氧气的物质的量是0.1mol,氧气中的O元素来自-1价的过氧化氢,所以转移电子的数目是0.2NA,错误;B、氧化铝还可与碱反应盐和水,所以氧化铝是两性氧化物,错误;C、氯化铵溶液中,铵根离子发生水解反应,存在水解平衡,水存在电离平衡,正确;D、电解质导电的过程中也有新物质生成,所以属于化学变化,错误,答案选C。
考点:考查阿伏伽德罗常数与电子数的关系,物质分类的判断,平衡的判断,物理变化、化学变化的判断
2、设阿伏加德罗常数的数值为NA,下列说法正确的是
A.80mL 10mol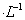 浓盐酸与足量MnO2反应,转移电子数为0.4NA
浓盐酸与足量MnO2反应,转移电子数为0.4NA
B.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为2NA
C.1 mol A13+含有核外电子数为3NA
D.常温下,16g CH4中共用电子对的数目为4NA
【知识点】物质的量单元测试
【答案】
D
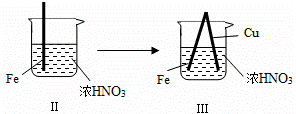
3、在通风橱中进行下列实验:
| 步骤 | 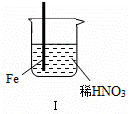
| 
|
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
下列说法不正确的是( )
A.Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2
B.Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应
C.对此Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3
D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化
【知识点】金属元素的单质及其化合物
【答案】
【考点】真题集萃;氧化还原反应;硝酸的化学性质.
【分析】A.硝酸具有强氧化性,与Fe反应生成NO,NO遇空气变为二氧化氮;
B.浓硝酸具有强氧化性,Fe表面形成致密的氧化层,发生钝化现象;
C.对比I、Ⅱ的现象,Fe与稀硝酸反应生成NO,而Fe与浓硝酸反应生成二氧化氮且迅速被钝化,说明浓硝酸的氧化性强于稀硝酸;
D.根据Ⅲ中现象,说明构成原电池,在Fe、Cu之间连接电流计,通过电流计指针偏转,可以判断原电池的正负极.
【解答】解:A.稀硝酸具有酸性与强氧化性,与Fe反应生成NO,NO遇空气变为二氧化氮,Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2═2NO2,故A正确;
B.Ⅱ的现象是因为铁发生了钝化,Fe表面形成致密的氧化层,阻止Fe进一步反应,故B正确;
C.对比I、Ⅱ的现象,Fe与稀硝酸反应生成NO,而Fe与浓硝酸反应生成二氧化氮且迅速被钝化,说明浓硝酸的氧化性强于稀硝酸,故C错误;
D.根据Ⅲ中现象,说明构成原电池,在Fe、Cu之间连接电流计,通过电流计指针偏转,可以判断原电池的正负极,进而判断Fe是否被氧化,故D正确,
故选:C.
【点评】本题考查硝酸的化学性质、原电池原理,难度不大,侧重考查学生分析解决问题的能力.













