
六盘水美术生文化课补习中心大概收费?
1、 这个学校位置还是好找。进门就有老师接待,咨询老师很专业,建议的课程也很符合娃娃的情况,感觉很正规。教室还挺多,环境还是挺干净的,看起来很敞亮。在网上看到来体验一下,老师帮忙安排了试听,上课老师课程安排很有趣,娃娃很喜欢,这一趟没有白来,很开心
2、 选择了新学高考是因为,老师很负责,非常认真,离家很近。老师经常会做出针对孩子短板的辅导,也会出许多重点难点问题的专项练习和辅导。
3、亲戚介绍过来的新学高考,孩子成绩一直不稳定,高三了想要冲刺个好大学,就去体验了一节课,孩子觉得不错,老师也很专业。
 六盘水美术生文化课补习中心大概收费
六盘水美术生文化课补习中心大概收费 招生详情:班型开设“名校冲刺班”、“理综加强班”、“高考冲刺”等。新学高考现招收达到我校招生要求的学生。新学高考艺考生报名时间从即日起可来电详询。
【专业的师资管理团队】
整合了西南地区知名的教育专家、名校的金牌讲师,教育心理学硕士、高考艺考生补习专家、高考全日制班级金牌管理组、
 六盘水美术生文化课补习中心大概收费
六盘水美术生文化课补习中心大概收费习题
1、右表为元素周期表前四周期的一部分,下列有关
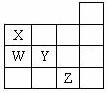 W、X、Y、Z四种元素的叙述中,正确的是
W、X、Y、Z四种元素的叙述中,正确的是
A.与氢原子形成的化学键的键能:W比Y的大
B.与氢原子形成的化学键的极性:X比Y的弱
C.低价气态氢化物的沸点:X的比W的高
D.XZ3的晶体属于离子晶体
【知识点】物质的量单元测试
【答案】
【答案】C
【解析】根据元素周期表的结构,X、W、Y、Z分别为N、P、S、Br,则由于氨气分子之间存在氢键,C正确.
2、某Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L﹣1的盐酸,测得溶液中的CO32﹣、HCO3﹣、AlO2﹣、Al3+离子的物质的量与加入盐酸溶液的体积变化关系如图所示,则下列说法正确的是( )

A.原混合溶液中的CO2﹣3与AlO﹣2的物质的量之比为1:2
B.V1:V2=1:5
C.M点时生成的CO2为0.05mol
D.a曲线表示的离子方程式为:AlO﹣2+H++H2O=Al(OH)3↓
【知识点】镁和铝
【答案】
【考点】镁、铝的重要化合物;钠的重要化合物;有关混合物反应的计算.
【专题】计算题;元素及其化合物.
【分析】Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L﹣1的盐酸.
首先,发生反应AlO2﹣+H++H2O═Al(OH)3↓,a线表示AlO2﹣,由图可知AlO2﹣反应完毕,加入盐酸50mL,根据方程式可知n(AlO2﹣)=n(H+)=0.05L×1mol/L=0.05mol.
第二阶段,AlO2﹣反应完毕,发生反应CO32﹣+H+═HCO3﹣,b线表示CO32﹣,c线表示HCO3﹣,由图可知CO32﹣反应完毕,该阶段加入盐酸100mL﹣50mL=50mL,根据方程式可知n(CO32﹣)=n(H+)=0.05L×1mol/L=0.05mol.
第三阶段,CO32﹣反应完毕,发生反应HCO3﹣+H+═CO2↑+H2O,d线表示HCO3﹣,由图可知HCO3﹣反应完毕,该阶段加入盐酸150mL﹣100mL=50mL,根据方程式可知n(HCO3﹣)=n(H+).
第四阶段,发生反应Al(OH)3+3H+═Al3++3H2O,e线表示Al3+,由图可知Al(OH)3反应完毕,根据方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,该阶段加入盐酸体积为 =0.15L=150mL.
=0.15L=150mL.
据此结合选项解答.
【解答】解:Na2CO3、NaAlO2的混合溶液中逐滴加入1mol•L﹣1的盐酸.
首先,发生反应AlO2﹣+H++H2O═Al(OH)3↓,a线表示AlO2﹣,由图可知AlO2﹣反应完毕,加入盐酸50mL,根据方程式可知n(AlO2﹣)=n(H+)=0.05L×1mol/L=0.05mol.
第二阶段,AlO2﹣反应完毕,发生反应CO32﹣+H+═HCO3﹣,b线表示CO32﹣,c线表示HCO3﹣,由图可知CO32﹣反应完毕,该阶段加入盐酸100mL﹣50mL=50mL,根据方程式可知n(CO32﹣)=n(H+)=0.05L×1mol/L=0.05mol.
第三阶段,CO32﹣反应完毕,发生反应HCO3﹣+H+═CO2↑+H2O,d线表示HCO3﹣,由图可知HCO3﹣反应完毕,该阶段加入盐酸150mL﹣100mL=50mL,根据方程式可知n(HCO3﹣)=n(H+).
第四阶段,发生反应Al(OH)3+3H+═Al3++3H2O,e线表示Al3+,由图可知Al(OH)3反应完毕,根据方程式可知n(H+)=3n[Al(OH)3]=3×0.05mol=0.15mol,该阶段加入盐酸体积为 =0.15L=150mL.
=0.15L=150mL.
A、由上述分析可知,原混合溶液中的CO32﹣与AlO﹣2的物质的量之比为0.05mol:0.05mol=1:1,故A错误;
B、原溶液中n(CO32﹣)=0.05mol,V1时溶液中碳酸氢根离子等于碳酸根离子为0.025ml,由反应CO32﹣+H+═HCO3﹣可知,需要盐酸为0.025mol,盐酸的体积为 =0.025L=25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,故B错误;
=0.025L=25mL,故V1=50mL+25mL=75mL,由上述分析可知,V2=150mL+150mL=300mL,故V1:V2=75mL:300mL=l:4,故B错误;
C、由上述分析可知M点时溶液中CO32﹣完全转化为HCO3﹣,没有CO2生成,故C错误;
D、由上述分析可知,a曲线表示的离子方程式为:AlO﹣2+H++H2O=Al(OH)3↓,故D正确.
故选:D.
【点评】考查离子反应与图象关系、化学计算等,难度中等,清楚离子反应的先后顺序是解题的关键.
3、已知R2+离子核外有a个电子,b个中子。表示R原子符号正确的是
A. B.
B. C.
C. D.
D.
【知识点】原子结构
【答案】
【知识点】原子的结构
【答案解析】D 解析:R2+离子核外有a个电子即R原子中有a+2个质子,b个中子即R原子中的质量数为a+b+2,故原子符号正确的为D。
【思路点拨】本题考查了在原子结构中质子数、中子数和质量数之间的关系,难度不大。











 W、X、Y、Z四种元素的叙述中,正确的是
W、X、Y、Z四种元素的叙述中,正确的是








