 四川艺考生培训文化课好的机构介绍
四川艺考生培训文化课好的机构介绍 教学方法:
配合TLE教学法。新学高考从考生心理、学习情况、身心健康、掌握程度等全方位优化其学习方法,激发艺考生学习斗志,让考生调整好心态,从容面对高考。战胜高考前的重重阻碍
【师资设置】
新学高考高三艺考生文化课补习班的教师队伍是由优秀教师、资深班主任、管理人员组建的专业教学团队。我们保证学生在学校接受的是优质的教育资源,先进的教育方式,科学的学习系统,决战2020高考,我们势必达成!!
 四川艺考生培训文化课好的机构介绍
四川艺考生培训文化课好的机构介绍 去年来是刘老师接待的我们,带我们参观了校区,关心的还是师资,通过试听娃娃反馈挺好的,说老师上课很有意思,也能学到东西。
在新学高考还没有学多久,感觉孩子变化大的就是学习积极性提高了很多,之前去补课都是闷闷不乐,但每次去新学高考就很开心,还主动提醒我注意时间不要迟到。老师很负责,家长有什么问题空了都会回复,值得推荐
孩子现在高三,面临毕业,正好近在找给孩子补习的地方,就在网上了解到了新学高考,当时接待我们的咨询老师非常专业,对高考政策非常熟悉以及中考的考纲考点也非常清楚,针对孩子的分数做了全方面分析,瞬间感觉升学道路清晰了很多,终决定尝试一下,希望孩子高考能有一个满意的分数。
 四川艺考生培训文化课好的机构介绍
四川艺考生培训文化课好的机构介绍 1、在0.01 mol·L-1 H2SO4溶液中,水电离出的H+浓度为( )
A.1×10-12 mol·L-1 B.1×10-7 mol·L-1
C.5×10-13 mol·L-1 D.5×10-12 mol·L-1
【知识点】水的电离和溶液的PH
【答案】
解析 0.01 mol·L-1的H2SO4溶液中c(H+)=0.02 mol·L-1,c(OH-)=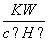 =
=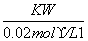 =5×10-13 mol·L-1,该溶液中水电离出的c(H+)等于溶液中c(OH-)。
=5×10-13 mol·L-1,该溶液中水电离出的c(H+)等于溶液中c(OH-)。
答案 C
2、已知NaHC2O4溶液显弱酸性,向100mL0.1mol•L﹣1的NaHC2O4.溶液中分别加入下列物质,有关说法正确的是()
A. 加入少量H2 C2O4固体,促进水电离,溶液中c(H+)增大
B. 加入NaOH溶液至恰好完全反应,则溶液中:c(Na+)>c(C2O42﹣)>c(HC2O4﹣)>c(H+)
C. 加入氨水至中性,则溶液中:c(NH4+)+c(Na+)=2c(C2O42﹣)+c(HC2O4﹣)
D. 加入0.01 mol Na2C2O4固体,则溶液中:3c(Na+)=2
【知识点】盐类的水解
【答案】
考点: 离子浓度大小的比较.
分析: NaHC2O4溶液显弱酸性,说明HC2O4﹣的电离程度大于其水解程度,
A.加入H2C2O4固体后,溶液中氢离子浓度增大,抑制了水的电离;
B.恰好反应后生成Na2C2O4,C2O42﹣部分水解,溶液显示碱性,由于氢离子来自水的电离和C2O42﹣的水解,则c(H+)>c(HC2O4﹣);
C.溶液为中性,则c(H+)>c(OH﹣),根据溶液中的电荷守恒判断;
D.根据混合液中的物料守恒分析.
解答: 解:NaHC2O4溶液显弱酸性,说明HC2O4﹣的电离程度大于其水解程度,
A.酸溶液抑制了水的电离,加入H2C2O4固体后,溶液中氢离子浓度增大,则水的电离程度减小,抑制了水的电离,故A错误;
B.加入NaOH溶液至恰好完全反应生成Na2C2O4,C2O42﹣部分水解,溶液显示碱性,由于氢离子来自水的电离和C2O42﹣的水解,则c(H+)>c(HC2O4﹣),正确的离子浓度大小为:c(Na+)>c(C2O42﹣)>c(H+)>c(HC2O4﹣),故B错误;
C.中性溶液中c(H+)>c(OH﹣),根据电荷守恒可得:c(NH4+)+c(Na+)=2c(C2O42﹣)+c(HC2O4﹣),故C正确;
D.加入0.01 mol Na2C2O4固体,混合液中含有等浓度的Na2C2O4和NaHC2O4,根据物料守恒可得:2c(Na+)=3,故D错误;
故选C.
点评: 本题考查了离子浓度大小比较,题目难度中等,明确电荷守恒、物料守恒及盐的水解原理为解答关键,注意掌握判断离子浓度大小常用方法,试题培养了学生的分析、理解能力及灵活应用基础知识的能力.
3、某有机物的结构为下图所示,这种有机物不可能具有的性质是( )
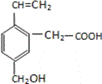
①所有碳原子可能共面;
②能使酸性KMnO4 溶液和溴水褪色,且原理相同;
③1mol 该有机物分别与足量 Na 或NaHCO3 反应,产生气体在标况下体积不相等;
④能发生酯化反应;
⑤能发生加聚反应;
⑥1mol 该有机物完全燃烧生成 CO2 和H2O 消耗 O2 的体积为 280L(标准状况)
A. ①② B. ②⑥ C. ③⑥ D. ②③
【知识点】烃的衍生物单元测试
【答案】
D
【解析】①有机物结构中苯环、双键为平面结构,与苯环、双键直接相连的原子一定共面,则分子中所在的碳原子可能共面,故不选①;
②该有机物合有碳碳双键,发生氧化反应使酸性KMnO4溶液褪色,使溴水褪色是发生加成反应,原理不同,故选②;
③-COOH、-OH均可与Na反应生成氢气,则1mol该有机物与足量Na反应生成1mol氢气;与NaHCO3反应的只有-COOH,1mol该有机物与足量-COOH反应生成1mol二氧化碳,在相同条件下,气体体积相同,故选③;
④该有机物含有羧基,羟基,可以发生酯化反应,故不选④;
⑤该有机物含有碳碳双键,可以发生加聚反应,故不选⑤;
⑥该有机物分子式为C11H12O3,1mol该有机物完全燃烧生成CO2和H2O消耗O2的体积为(11+3-1.5)mol×22.4L/mol =280L,故不选⑥;
综上所述,应选②③,故答案为:D。












