 自贡艺考文化课冲刺学校哪里好
自贡艺考文化课冲刺学校哪里好 【新学高考优势】
1、我们会依据学生学习水平的差异化,来为学生制定自己专属的学习方案。
2、教学方法显著,重视老师与学生之间的沟通和交心,使老师成为学生学习上的引路人。
3、新学高考提供一对一补习,在各方面、各维度中解决学生的困扰,帮助学生能更快的提高成绩。
【新学高考管理模式】
我们的老师会定期一对一与同学们进行沟通,让同学们树立信心,适当加压及增进动力,改进学习方法,制订目标;平时主题活动、体育活动、心理辅导保持备考阶段心态的平稳。
 自贡艺考文化课冲刺学校哪里好
自贡艺考文化课冲刺学校哪里好 教师亲切负责,教学水平高,孩子积极肯学,学管师负责贴心,监督到位,只是针对性强,学习了一学期后提分效果显著,孩子反映上课气氛活跃,同学友好,理科补课的多一些,。价格收费合理,现在搬了新校区,环境不错哦。
在家附近咨询了很多地方,后选择了新学高考,我孩子现在学习上自律性较差,找不到学习方法。第一次带去咨询接待我们的是陈老师,陈老师很专业讲得很耐心,很有亲和力!我孩子也很喜欢在这里学习,体验了几节课后给孩子报了一对一课程。
孩子的数学成绩很不好,就在新学高考学习报了小班补习,在了解孩子学习情况后,老师为孩子制定了学习计划,不到两个月,数学成绩就飞速上升,连学校老师都不敢相信,新学高考的老师真厉害
 自贡艺考文化课冲刺学校哪里好
自贡艺考文化课冲刺学校哪里好 1、在恒温恒压下,向密闭容器中充入4mol A和2mol B,发生如下反应:2A(g)+B(g)⇌2C(g)△H<0
2min后,反应达到平衡,生成C为1.6mol.则下列分析正确的是( )
A.若反应开始时容器体积为2 L,则v(C)=0.4mol•L﹣1•min﹣1
B.若该反应在恒温恒容下进行,放出热量将增加
C.若2 min后,向容器中再投入等物质的量A、C,则B的转化率不变
D.若在恒压绝热条件下反应,平衡后n(C)<1.6mol
【知识点】化学平衡
【答案】
【考点】化学平衡的影响因素;化学平衡建立的过程.
【分析】A、依据化学反应速率=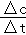 计算分析判断;
计算分析判断;
B、恒温恒容条件反应过程中,压强减小;
C、若2min后,向容器中再投入等物质的量A、C,平衡正向进行;
D、在恒压绝热条件下反应,反应放热,平衡逆向进行,平衡后n(C)<1.6mol.
【解答】解:A、由化学平衡三段式可知,
2A(g)+B(g)⇌2C(g)
起始量(mol) 4 2 0
变化量(mol) 1.6 0.8 1.6
平衡量(mol) 2.4 1.2 1.6
若反应开始时容器体积为2L,平衡后容器体积小于2L,则v(C)>0.4mol/(L•min),故A错误;
B、恒温恒容条件反应过程中,压强减小,平衡逆向进行放出的热量减小,故B错误;
C、若2min后,向容器中再投入等物质的量A、C,平衡正向进行,B的转化率增大,故C错误;
D、依据平衡计算,在恒压绝热条件下反应,反应是放热反应,温度升高平衡逆向进行,平衡后n(C)<1.6mol,故D正确;
故选D.
【点评】本题考查了化学平衡的影响因素分析判断,注意恒温恒容、恒温恒压条件下分析的角度不同,结果不同,注意掌握平衡移动原理的实质应用,题目难度中等.
2、下列 实验方法正确的是
实验方法正确的是
A.除去NaCl固体中少量的NH4Cl,可用加热的方法除去
B.除去NO2气体中少量的NO气体,可通入适量的O2
C.除去FeSO4溶液中少量的Fe2(SO4)3,可加入Cu粉充分反应后过滤
D.除去NaHCO3固体中少量的Na2CO3,可用加热至恒重的方法除去
【知识点】几种重要的金属单元测试
【答案】
A
3、下列表述正确的是
①浓硝酸通常保存在棕色试剂瓶中
②检验亚硫酸钠溶液在空气中放置是否变质可以先加硝酸溶液,再加氯化钡溶液来检验
③锌与稀硝酸反应可以得到氢气
④足量铁与稀硝酸反应后溶液呈浅绿色,说明稀硝酸不能氧化Fe2+
⑤ 浓硫酸滴到纸张上变黑,说明浓硫酸具有吸水性
⑥二氧化硫和二氧化氮都能形成酸雨,酸雨的pH等于5.6
A.①③④ B.①② C.① D.①②⑤⑥
【知识点】非金属元素的单质及其化合物
【答案】
C











