 简阳音乐生文化课集训中心排名
简阳音乐生文化课集训中心排名 【新学高考优势】
1.深度解析学习问题
不同的问题有不同的解决方法,我们因材施教。
2.7x24小时学习管理
任课老师+班主任实时掌握孩子学习问题和学习动态,联合反馈。
3.课程安排时间灵活
根据孩子的时间安排上课时间段、时间点,真正做到灵活适应。
4.全科严选专职教师
专职教师严格选查,反复磨练。
【师资设置】
新学高考高三艺考生文化课补习班的教师队伍是由优秀教师、资深班主任、管理人员组建的专业教学团队。我们保证学生在学校接受的是优质的教育资源,先进的教育方式,科学的学习系统,决战2020高考,我们势必达成!!
 简阳音乐生文化课集训中心排名
简阳音乐生文化课集训中心排名 就在这家机构给孩子报了高三全科辅导课程,孩子的进步很快,而且还对初一知识进行回顾学习,效果提升真的很快,老师的教学方法很给力!
如果要我推荐一个高考补习学校,我会首先推荐新学高考的,为什么呢?因为我家小孩就是在这里补习过的,补习的效果是很明显的好,成绩提上去了,就是这个学校好的证明,所以我才愿意推荐。
孩子上高三了,过来体验了这个学校的课程,去看了很多地方,还是满意这里,主要是觉得这个地方的老师非常认真负责,随时可以交流沟通孩子的学习情况,有什么问题也会马上跟我们家长联系,学校的环境也很不错﹐推荐给大家哈!
 简阳音乐生文化课集训中心排名
简阳音乐生文化课集训中心排名 1、用NA表示阿伏德罗常数,下列叙述正确的是( )
A.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl﹣个数为NA
B.常温常压下,1.06g Na2CO3含有的Na+离子数为0.01NA
C.通常状况下,NA个CO2分子占有的体积约为22.4L
D.氧气和臭氧的混合物16 g中约含有NA个氧原子
【知识点】物质的量单元测试
【答案】
【考点】阿伏加德罗常数.
【专题】阿伏加德罗常数和阿伏加德罗定律.
【分析】A、溶液体积不明确;
B、求出碳酸钠的物质的量,然后根据1mol碳酸钠中含2mol钠离子来分析;
C、通常状况下,气体摩尔体积大于22.4L/mol;
D、氧气和臭氧均由氧原子构成.
【解答】解:A、溶液体积不明确,故溶液中的氯离子的个数无法计算,故A错误;
B、1.06g碳酸钠的物质的量为0.01mol,而1mol碳酸钠中含2mol钠离子,故0.01mol碳酸钠中含0.02mol钠离子即0.02NA个,故B错误;
C、通常状况下,气体摩尔体积大于22.4L/mol,故NA个二氧化碳分子的物质的量为1mol,则所占的体积大于22.4L,故C错误;
D、氧气和臭氧均由氧原子构成,故16g混合物中含有的氧原子的物质的量n=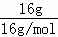 =1mol,个数为NA个,故D正确.
=1mol,个数为NA个,故D正确.
故选D.
【点评】本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.
2、用NA表示阿伏加德罗常数的值.下列说法正确的是( )
A.7.1gCl2与足量的氢氧化钠溶液反应转移的电子数一定为0.2NA
B.在常温常压下,11.2 升氯气含有的分子数为0.5NA
C.常温常压下,32 g O2和O3的混合气体所含原子数为2NA
D.1 molFe与足量的Cl2反应转移的电子数为2NA
【知识点】物质的量单元测试
【答案】
【考点】阿伏加德罗常数.
【专题】阿伏加德罗常数和阿伏加德罗定律.
【分析】A、求出氯气的物质的量,然后根据氯气和碱的反应为歧化反应来分析;
B、常温常压下,气体摩尔体积大于22.4L/mol;
C、氧气和臭氧均由氧原子构成;
D、铁与氯气反应后变为+3价.
【解答】解:A、7.1g氯气的物质的量为0.1mol,而氯气和碱的反应为歧化反应,故0.1mol氯气转移0.1mol电子即0.1NA个,故A错误;
B、常温常压下,气体摩尔体积大于22.4L/mol,故11.2L氯气的物质的量小于0.5mol,故含有的分子数小于0.5NA个,故B错误;
C、氧气和臭氧均由氧原子构成,故32g氧气和臭氧中含有的氧原子的物质的量为n=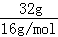 =2mol,故为2NA个,故C正确;
=2mol,故为2NA个,故C正确;
D、铁与氯气反应后变为+3价,故1mol铁与氯气反应后转移3mol电子即3NA个,故D错误.
故选C.
【点评】本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.
3、某温度下的某容积不变的密闭容器中,建立下列化学平衡:C(s)+H2O(g)  CO(g)+H2(g)不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
CO(g)+H2(g)不能确定上述可逆反应在一定条件下已达到化学平衡状态的是( )
A.体系的压强不再发生变化 B.v正(CO)=v逆(H2O)
C.生成n mol CO的同时生成n mol H2
D.1 mol H—H键断裂的同时断裂2 mol H—O键
【知识点】化学反应速率 化学平衡
【答案】
C



















