 万源艺体生文化课辅导学校排名
万源艺体生文化课辅导学校排名 新学高考优势:
学生生活起居:为保证学生的身体健康,营养跟上,学生的三餐所吃的食物都是由营养管理师精心搭配,
学生住宿条件:24小时热水、空调、洗衣机、一应俱全
学生教学环境:教室宽敞明亮,新式课桌配套,给学生打造一个舒适的学习空间
【新学高考管理模式】
教师坐班,随时能找老师答疑问题,尽快解决每个疑问,不留问题到明天,提高学习效率和质量;教师坐班,能够让学生体会到教师与他们同进退,教师不仅仅是良师,还是益友;学科间教师互相讨论,统筹教学规划、分析学生学习情况,及时调整教学内容。
新学高考全日制冲刺辅导,为学生的成长保驾护航!新学高考愿帮助很更多的学生实现自己的梦想!
 万源艺体生文化课辅导学校排名
万源艺体生文化课辅导学校排名 体验过后感觉自己有了一定的提升,并且许多缺少的知识都得到了相对的补充。老师授课很认真,并且思路非常清晰,还能关注到每一位学生。
在培训机构行业里新学高考算是比较大的一家了。对于新学高考的从业人员来说,他们的选拔要求也是挺高的。自己就很不幸的,没有成功入选。他们的教学态度和师资的力量还是非常不错的
这家补习机构真心不错,老师很负责任,不仅仅是补习文化课,更多能够让孩子养成好的学习习惯,对娃娃很上心,我们这些做家长的把孩子放在x新学补习是很好的选择了,补了快半年了,娃娃能够主动自己去上课,成绩也有所提升,推荐大家可以试试,补习机构一定要多选择,合适自己的孩子重要,不然就是浪费家长的精力,希望孩子能够考一个好大学。
 万源艺体生文化课辅导学校排名
万源艺体生文化课辅导学校排名 1、能证明胶体微粒比溶液中电解质微粒大的操作是( )
A.丁达尔效应 B.布朗运动 C.渗析 D.电泳现象
【知识点】电化学 胶体
【答案】
C
2、部分弱酸的电离平衡常数如下表:下列说法正确的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 | K=1.77×10﹣4 | K=4.9×10﹣10 | K1=4.2×10﹣7 K2=5.6×10﹣11 |
A.0.1mol•L﹣1NaHCO3溶液中浓度的大小:c(Na+)>c(HCO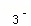 )>c(H+)>c(OH﹣)
)>c(H+)>c(OH﹣)
B.少量的CO2通入到NaCN溶液中 CN﹣+H2O+CO2=HCN+HCO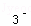
C.用0.1mol•L﹣1NaOH溶液中和等浓度的HCN和HCOOH时前者所需NaOH溶液体积大
D.0.1mol•L﹣1HCOONa溶液比0.1mol•L﹣1NaCN溶液所含离子总数小
【知识点】电离平衡单元测试
【答案】
【考点】弱电解质在水溶液中的电离平衡.
【分析】A、碳酸氢钠中碳酸氢根离子水解程度大于电离程度而使其溶液呈碱性;
B、碳酸的酸性比HCN强,少量二氧化碳通入NaCN溶液中,生成碳酸氢根;
C、中和碱的能力与酸性强弱无关;
D、没有指明溶液体积,无法比较离子数目多少.
【解答】解:A、碳酸氢钠中碳酸氢根离子水解程度大于电离程度而使其溶液呈碱性,所以c(H+)<c(OH﹣),故A错误;
B、碳酸的酸性比HCN强,少量二氧化碳通入NaCN溶液中,生成碳酸氢根,其离子方程式为:CN﹣+H2O+CO2=HCN+HCO3﹣,故B正确;
C、相同物质的量的HCN和HCOOH,中和碱的能力相同,元数相同的酸中,酸中和碱的能力与酸的物质的量成正比,与酸的强弱无关,所以用0.1mol•L﹣1 NaOH溶液中和等浓度的HCN和HCOOH时,二者需要NaOH溶液体积相等,故C错误;
D、没有指明溶液体积,无法比较离子数目多少,故D错误;
故选B.
【点评】本题考查了弱电解质的电离及盐类水解,明确弱酸的电离平衡常数与酸性强弱、酸根离子水解程度之间的关系即可解答,易错选项是C,题目难度不大.
3、下列说法正确的是( )
A.任何酸与碱发生中和反应生成1 mol H2O的过程中,能量变化均相同
B.同温同压下,H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下的ΔH不同
C.已知:①2H2(g)+O2(g)===2H2O(g)
ΔH=-a kJ·mol-1,
②2H2(g)+O2(g)===2H2O(l)
ΔH=-b kJ·mol-1,则a>b
D.已知:①C(s,石墨)+O2(g)===CO2(g)
ΔH=-393.5 kJ·mol-1,
②C(s,金刚石)+O2(g)===CO2(g)
ΔH=-395.0 kJ·mol-1,
则C(s,石墨)===C(s,金刚石) ΔH=+1.5 kJ·mol-1
【知识点】燃烧热和中和热
【答案】
【解析】 A项,酸、碱强弱不同,反应过程的能量变化不同;B项,反应的ΔH与反应条件无关;C项,a<b;D项,利用①-②可得。
【答案】 D



















