
毕节音乐生文化课辅导机构有哪些?
1、 新学高考在高三辅导机构里面还是不错的,很多老师的教龄都超过了10年,希望孩子在这里能有好收获
2、 很不错,孩子有了很好的进步。以为老师每天的反馈孩子的学习情况不会持续太久,谁知到一直持续到我孩子上完整个课程。为老师们点赞。
3、 环境不错,老师也很有经验,娃娃能够很快进入学习状态。今天刚试听一次课,娃娃就说要在新学上课了。希望能够取得进步
 毕节音乐生文化课辅导机构有哪些
毕节音乐生文化课辅导机构有哪些 【开设班型】
新学高考开班时间随到随学,滚动开班。在传统分班,分文科班型和理科班型的前提下。班型的设置更加合理化:设有文科一对一班、理科一对一班、理科精品小班、文科精品小班。
新学高考艺考生中心师资介绍
新学高考艺考生中心的师资自是不必多说,我们有资本说我们的老师都是行业内佼佼者,我们的老师都是具备丰厚的专业知识,从教年龄亦是不可小觑,我们有众多一线公立学校挖过来的的优秀教师,也有学校从各个名校招聘的专业教师,专注高考辅导,针对艺考生的短板更是自有一套方法。
 毕节音乐生文化课辅导机构有哪些
毕节音乐生文化课辅导机构有哪些习题
1、结合图判断,下列叙述正确的是( )
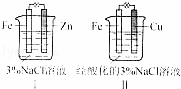
A.Ⅰ是验证牺牲阳极的阴极保护法的实验装置
B.Ⅰ和Ⅱ中负极反应均是Fe﹣2e﹣=Fe2+
C.Ⅰ和Ⅱ中正极反应均是O2+2H2O+4e﹣=4OH﹣
D.Ⅰ和Ⅱ中分别加入少量K3Fe(CN)6溶液,均有蓝色沉淀
【知识点】电化学 胶体
【答案】
考点:原电池和电解池的工作原理.
专题:电化学专题.
分析:A、Ⅰ装置是原电池,锌做负极,铁做正极,发生的是锌的吸氧腐蚀;
B、Ⅰ中原电池负极为锌,Ⅱ为原电池,铁做负极;
C、Ⅰ装置是电解质溶液时中性溶液,属于吸氧腐蚀,Ⅱ装置中电解质溶液时酸性溶液,属于析氢腐蚀;
D、Ⅰ装置中不能生成亚铁离子,Ⅱ装置中负极铁失电子生成亚铁离子.
解答: 解:A、Ⅰ装置是原电池,锌做负极,铁做正极,发生的是锌的吸氧腐蚀,是验证牺牲阳极的阴极保护法的实验装置,故A正确;
B、Ⅰ中原电池负极为锌,电极反应为Zn﹣2e﹣=Zn2+,Ⅱ为原电池,铁做负极,电极反应为Fe﹣2e﹣=Fe2+,故B错误;
C、Ⅰ装置是电解质溶液时中性溶液,属于吸氧腐蚀,正极电极反应为:O2+2H2O+4e﹣=4OH﹣,Ⅱ装置中电解质溶液时酸性溶液,属于析氢腐蚀,正极电极反应为2H++2e﹣=H2↑,故C错误;
D、加入少量K3Fe(CN)6溶液,有蓝色沉淀是亚铁离子的性质,Ⅰ装置中不能生成亚铁离子,Ⅱ装置中负极铁失电子生成亚铁离子,故D错误;
故选A.
点评:本题考查了原电池原理的分析判断,注意电解质溶液不同,电极与电极反应变化,掌握基础是关键,题目难度中等.
2、反应N2O4(g) 2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A深,C浅
C.由状态B到状态A,可以用加热的方法
D.A、C两点气体的平均相对分子质量:A>C

【知识点】化学平衡单元测试
【答案】
C
3、含11.2g KOH的稀溶液与1L 0.1mol/L的H2SO4溶液反应放出11.46kJ的热量,下列能正确表示中和热的热化学方程式是()
A. KOH(aq)+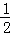 H2SO4(aq)=1/2K2SO4(aq)+H2O (l);△H=﹣11.46kJ/mol
H2SO4(aq)=1/2K2SO4(aq)+H2O (l);△H=﹣11.46kJ/mol
B. 2KOH(s)+H2SO4(aq)=K2SO4(aq)+2H2O (l);△H=﹣114.6kJ/mol
C. 2KOH(aq)+H2SO4=K2SO4(aq)+H2O (l);△H=+114.6kJ/mol
D. KOH (aq)+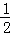 H2SO4(aq)=
H2SO4(aq)=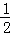 K2SO4(aq)+H2O (l);△H=﹣57.3kJ/mol
K2SO4(aq)+H2O (l);△H=﹣57.3kJ/mol
【知识点】化学反应中的能量变化
【答案】
考点: 中和热.
分析: 根据酸碱的物质的量判断反应的情况,根据中和热是指稀的强酸和强碱反应生成1mol水所放出的热量来书写中和热的热化学方程式.
解答: 解:11.2g即0.2molKOH的稀溶液与1L、0.1mol/L的H2SO4溶液反应放出11.46kJ的热量,实质是生成0.2mol水放出11.46kJ的热量,而中和热的热化学方程式必须保持生成水的物质的量为1mol.
A、生成1mol水放出的热量会高于11.46kJ,故A错误;
B、氢氧化钾应是溶液,不是固体,故B错误;
C、中和反应是放热反应,不是吸热反应,故C错误;
D、KOH的稀溶液与H2SO4溶液反应生成0.2mol水放出11.46kJ的热量,生成1mol水会放出57.3KJ的能量,故D正确.
故选D.
点评: 本题考查中和热的概念以及热化学方程式的含义,可以根据所学知识来回答,难度不大.













