
安顺音乐生文化课辅导班前三?
1、新学高考学校环境很好,老师也非常的专业,入学的时候会有测评,找到了孩子目前学习上的很多问题,还给我讲了一下之后如何改正这些问题,课程应该如何规划,真是超级负责任!
2、 新学高考不管是硬件条件还是师资力量,总校都比较完备,交通也比较方便,学校的是全日制的那种,食宿一体化的,学校环境的也很干净,装修也挺好的。
3、 朋友推荐过来的,一开始也是抱着试试的态度,但是过来上了体验果之后才发现这边的老师真的很专业,很耐心,很负责,可以把娃儿的问题点一针见血的指出来,比之前很多地方都要好太多了。这几次考试都有进步,真的很感谢各位老师们!希望娃儿可以在这里收获更多
 安顺音乐生文化课辅导班前三
安顺音乐生文化课辅导班前三 高三艺考生文化课补习班介绍:
全封闭式班型开课时间:随到随学 滚动开班
全封闭式管理模式:食宿一体 周一至周六全天上课 每周休息一天,早上6:00起床,晚上23:00休息。
全封闭式收费标准:按照学生选择的班型和课时决定,详情来电咨询
实力告诉艺考生和家长为什么选择新学高考
我们是正规学校,拥有教育局发放的民办学校资质。
校区设立在城区,新学高考实行全封闭式管理,教学楼,宿舍,食堂,操场,教学环境,硬件设施都非常好。这对于艺考生的学习环境和学习效率有很大帮助
新学高考根据每个艺考生的情况不同,实行差异化针对性教学。入学前可根据家长和艺考生的意愿选择班型。
【新学高考管理制度】
每班配备专职班主任,关注和管理每班师生的上课情况与安全,每天点名、签到,如出现迟到、旷课情况及时和家长电话沟通,并反馈学生听课学习情况,如家长发现不负责任的班主任,请及时联系学校办公室并及时处理。直到家长和学生满意。
 安顺音乐生文化课辅导班前三
安顺音乐生文化课辅导班前三习题
1、下列反应中属于消去反应的是( )
| | A. | 乙烯通入溴水溶液褪色 |
| | B. | 甲苯与浓硫酸和浓硝酸的反应 |
| | C. | 溴乙烷与NaOH醇溶液共热 |
| | D. | 甲烷与氯气在光照的条件下反应 |
【知识点】乙烯 烯烃
【答案】
考点:
消去反应与水解反应. | | 专题: | 有机反应. |
| 分析: | 有机物中脱去一个或几个小分子(如水、卤化氢等分子),而生成不饱和(碳碳双键或三键或苯环状)化合物的反应,叫做消去反应,结合有机物结构判断. |
| 解答: | 解:A.乙烯与溴水发生加成反应生成1,2﹣二溴乙烷,故A不符合; B.甲苯与浓硫酸和浓硝酸的反应,苯环中H原子被硝基取代生成硝基苯,属于取代反应,故B不符合; C.CH3CH2Br脱去一个HBr,生成不饱和的CH2=CH2,属于消去反应,故C符合; D.甲烷与氯气在光照的条件下反应,氢原子被氯原子取代生成甲烷氯代物,属于取代反应,故D不符合; 故选C. |
| 点评: | 本题考查有机反应类型,难度不大,注意对有机反应概念的理解,注意从反应中反应物和生成物的结构理解有机反应类型. |
2、含有下列各组离子的溶液中,通入过量SO2气体后仍能大量共存的是
A. H+、Ca2+、Fe3+、NO3- B. Ba2+、Cl-、AlO2-、OH-
C. Na+、NH4+、I-、HS- D. Na+、Ca2+、K+、Cl-
【知识点】化学反应及其能量变化单元测试
【答案】
【答案】D
【解析】A.因足量SO2通入溶液时,SO2与Fe3+发生氧化还原反应,2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,则不能共存,选项A错误;B.因足量SO2通入溶液时,SO2与OH-反应,且反应生成的酸能与AlO2-反应生成氢氧化铝沉淀而使离子不能大量共存,选项B错误;C.因亚硫酸的酸性比氢硫酸强,所以当溶液中,通入过量SO2气体后,SO2+H2O⇌H2SO3,H2SO3⇌H++HSO3-,HSO3-⇌H++SO32-,H++HS-=H2S↑,2H2S+SO2=3S↓+2H2O则不能共存,选项C错误;D.该组离子不反应,能大量共存,溶液中,通入过量SO2气体后,SO2+H2O⇌H2SO3,H2SO3⇌H++HSO3-,HSO3-⇌H++SO32-,氢离子、亚硫酸根离子与Na+、Ca2+、K+、Cl-均不反应,也能大量共存,选项D正确。
3、四种短周期元素在周期表中的位置如右图,其中只有M为金属元素.下列说法不正确的是()
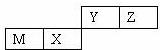
A. 原子半径Z<M
B. Y的高价氧化物对应水化物的酸性比X的弱
C. X的简单气态氢化物的热稳定性比Z的小
D. Z位于元素周期表中第2周期、第ⅥA族
【知识点】物质结构 元素周期律单元测试
【答案】
考点: 位置结构性质的相互关系应用.
专题: 元素周期律与元素周期表专题.
分析: 根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只有M为金属元素,掌握M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素,据此结合元素周期律解答.
解答: 解:根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只有M为金属元素,掌握M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径O<Al,故A正确;
B.非金属性N>Si,故酸性HNO3>H2SiO3,故B错误;
C.非金属性Si<O,故氢化物稳定性SiH4<H2O,故C正确;
D.Z为氧元素,位于元素周期表中第2周期第ⅥA族,故D正确;
故选B.
点评: 本题考查结构性质位置关系、元素周期律等,难度不大,推断元素是解题关键,注意对元素周期表的整体把握,注意对元素周期律的理解掌握.












