
毕节艺术生文化课集训中心推荐?
1、 带孩子去试听了一下,孩子马上高三了,学习要抓紧了,听她同学说新学还不错,也很多人来学习,所以今天感受了一下,老师讲解思路清晰,解题方法也容易理解,校区也挺大的,来往的学生也挺多,整体还不错!
2、 新学高考是老牌的大机构,孩子在这里学习很放心!教学质量也不错!
3、 亲戚介绍过来的,她的女儿就在这里补习,现在做题的速度正确路都很好,保持前几名并稳定。而我儿子的数学成绩一直都不稳定。下学期马上就上高三了,就在新学这里报了全日制的班,学校的老师还多负责的,老师也分析的很到位!
 毕节艺术生文化课集训中心推荐
毕节艺术生文化课集训中心推荐 新学高考艺考生课程详情:
【高考艺考生招生对象】应届生、艺考生、云贵川全国3卷考生
【新学高考艺考生文化课补习班开设班型】专属一对一、精品5人小班、精品9人中班
【新学高考管理模式】食宿一体制,学生入学就有老师24小时陪护,及时解决学生在学习过程中的任何问题
【新学高考艺考生文化课补习班收费】根据学生入学时选择的班型、老师、课时收费
【教研团队】
新学高考经过严格筛选的教研团队会定期组织教研活动,根据教学情况及时作出调整改善;定期举行专题研究,确保教学效果优化;组织高考押题研究活动,准确把握高考风向,多年压中高考题型,命中率高。
 毕节艺术生文化课集训中心推荐
毕节艺术生文化课集训中心推荐习题
1、研究电化学腐蚀及防护的装置如图所示。下列有关说法错误的是( )

A. d为石墨,铁片腐蚀加快
B. d为石墨,石墨上电极反应为:O2+2H2O+4e-=4OH-
C. d为锌块,铁片不易被腐蚀
D. d为锌块,铁片上电极反应为:2H++2e-=H2↑
【知识点】电化学 胶体
【答案】
【答案】D
【解析】
A、由于活动性:Fe>石墨,所以铁、石墨及海水构成原电池,Fe为负极,失去电子被氧化变为Fe2+进入溶液,溶解在海水中的氧气在正极石墨上得到电子被还原,比没有形成原电池时的速率快,选项A正确;B、d为石墨,由于是中性电解质,所以发生的是吸氧腐蚀,石墨上氧气得到电子,发生还原反应,电极反应为:O2 + 2H2O + 4e-→ 4OH–,选项B正确;C、若d为锌块,则由于金属活动性:Zn>Fe,Zn为原电池的负极,Fe为正极,首先被腐蚀的是Zn,铁得到保护,铁片不易被腐蚀,选项C正确;D、d为锌块,由于电解质为中性环境,发生的是吸氧腐蚀,在铁片上电极反应为:O2 + 2H2O + 4e-→ 4OH–,选项D错误。答案选D。
点睛:本题考查金属的电化学腐蚀及防护的知识。根据电极上得失电子判断正负极,再结合电极反应类型、电子流向来分析解答,熟记原电池原理,电极反应式的书写是本题解题的难点。
2、下列有水参加的化学反应中,不属于水解反应的是( )
| | A. | NH4++H2O⇌NH3•H2O+H+ | B. | HCO3﹣+H2O⇌H3O++CO32﹣ |
| | C. | Al3++3H2O⇌Al(OH)3+3H+ | D. | CH3COO﹣+H2O⇌CH3COOH+OH﹣ |
【知识点】盐类的水解
【答案】
考点:
盐类水解的原理. | | 专题: | 盐类的水解专题. |
| 分析: | A、反应中是铵根离子水解的反应; B、反应中是碳酸氢根离子电离的方程式,水是生成的氢离子水合离子形式,不属于水解反应; C、铝离子水解生成氢氧化铝和氢离子; D、醋酸根离子水解生成醋酸和氢氧根离子. |
| 解答: | 解:A、NH4++H2O⇌NH3•H2O+H+,铵根离子水解生成一水合氨和氢离子,水参加反应,故A不符合; B、HCO3﹣+H2O⇌H3O++CO32﹣,是碳酸氢根离子电离方程式,水是生成水合氢离子,不是水解,故B符合; C、Al3++3H2O⇌Al(OH)3+3H+是铝离子水解反应,水参与反应,故C不符合; D、CH3COO﹣+H2O⇌CH3COOH+OH﹣,醋酸根离子水解生成醋酸和氢氧根离子,水参与反应,故D不符合; 故选B. |
| 点评: | 本题考查了盐类水解分析判断,电离过程的应用,主要是水合氢离子的表示方法的应用,题目较简单. |
3、某待测溶液(阳离子为Na+)中可能含有SO42-、SO32-、NO3-、Cl-、Br-、CO32-、HCO3-中的一种或多种,进行如图所示的实验,每次实验所加试剂均过量,下列说法不正确的是( )
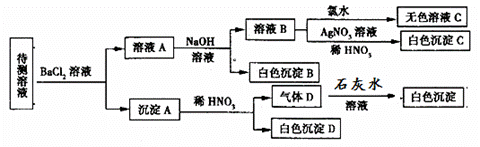
A.SO42-、SO32-至少含有一种
B.沉淀B的化学式为BaCO3
C.肯定存在的阴离子有CO32-、HCO3-、Cl-,还有SO42-、SO32-至少含有一种
D.肯定没有的离子是Br-
【知识点】离子反应
【答案】
【答案】C
【解析】待测液与氯化钡溶液反应生成沉淀A,则溶液中可能含有:CO32-、SO32-、SO42-,向沉淀中加入稀硝酸生成气体D,且有部分沉淀不溶解,则溶液中一定存在CO32-,溶液中可能存在SO32-、SO42-中的两种或一种;加入的氯化钡过量,所以滤液A中有Ba2+,滤液A中加入过量的NaOH溶液得到白色沉淀B,则溶液中一定含有HCO3-,白色沉淀B为BaCO3;滤液B中通入氯气,得无色溶液,溶液中一定不存在:S2-、Br-;滤液B中加入硝酸银、硝酸溶液得到白色沉淀,白色沉淀为AgCl,说明滤液B中含有Cl-,由于加入了氯化钡溶液,不能确定原溶液中是否含有Cl-。A、根据以上分析可知,待测液中至少存在SO32-、SO42-中的一种,正确;B、根据分析可知,气体D为CO2,沉淀B为碳酸氢根离子与钡离子、氢氧根离子反应生成的BaCO3,正确;C、根据分析可知待测液中Cl-不能确定是否存在,错误;D、根据分析可知待测液中一定不存在的离子为:S2-、Br-,正确。













