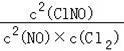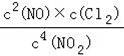黔南高考文化课辅导中心排名?
1、在外面学习首先就要找个管理严格的学校,我就是因为新学高考的管理严格规范,才过来的,过来学了有一段时间了,每天学习的时间几乎是生活的全部,我现在只想在这里安安心心的学习,考个好学校。
2、和其他机构对比了一下,环境还是很好的,主要是试听课孩子听的很认真,下来问了,孩子觉得自己是有收获的,也很喜欢这里的老师。
3、 新学高考的教学实力还是不错哒,提升还是挺明显,在努力一段时间,争取提升分数更高,谢谢老师们的帮助,我会继续努力的
 黔南高考文化课辅导中心排名
黔南高考文化课辅导中心排名 【新学高考艺考生文化课补习班型】
一对一个性化定制班型
5人精品小班
9人基础中班
【新学高考师资介绍】
新学高考教务老师是由几十位专门从事教育研究的老师们组成。他们精通高三学生学习问题,深谙其解决之道。能够帮助学生精准找到学习问题,明确涨分空间,为学生制定针对性的辅导方案。是学生学习重要的把关者。
 黔南高考文化课辅导中心排名
黔南高考文化课辅导中心排名习题
1、在恒温条件下,向盛有食盐的2L恒容密闭容器中加入0.2molNO2、0.2molNO和0.1molCl2,发生如下两个反应:
①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g)△H1<0 平衡常数K1
②2NO(g)+Cl2(g)⇌2ClNO(g)△H2<0 平衡常数K2
10min时反应达到平衡,测得容器内体系的压强减少20%,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10﹣3mol/(L•min).下列说法不正确的是( )
A.反应4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数为K12/K2
B.平衡后c(Cl2)=2.5×10﹣2mol/L
C.其它条件保持不变,反应在恒压条件下进行,则平衡常数K2增大
D.平衡时NO2的转化率为50%
【知识点】化学平衡
【答案】
【考点】CP:化学平衡的计算.
【分析】A.①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g),平衡常数K1=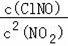
 ,
,
②2NO(g)+Cl2(g)⇌2ClNO(g),平衡常数K2 =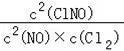
 ,
,
2×①﹣②可得4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g),进而计算平衡常数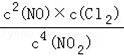
 ;
;
B.10min时反应达到平衡,测得容器内体系的压强减少20%,则平衡时混合气体总物质的量为(0.2+0.2+0.1)mol×(1﹣20%)=0.4mol,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10﹣3mol•L•min﹣1,则平衡时n(ClNO)=7.5×10﹣3mol•L•min﹣1×10min×2L=0.15mol,设①中反应的NO2为xmol,②中反应的Cl2为ymol,则:
2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g)
xmol 0.5xmol
2NO(g)+Cl2(g)═2ClNO(g)
2ymol ymol 2ymol
再根据ClNO物质的量与平衡时混合气体总物质的量列方程计算解答;
C.平衡常数只受温度影响,温度不变,则为平衡常数不变;
D.根据C中的计算结果,可以计算二氧化氮的转化率.
【解答】解:A.①2NO2(g)+NaCl(s)⇌NaNO3(s)+ClNO(g),平衡常数K1=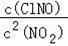
 ;
;
②2NO(g)+Cl2(g)⇌2ClNO(g),平衡常数K2 =

4NO2(g)+2NaCl(s)⇌2NaNO3(s)+2NO(g)+Cl2(g)的平衡常数K=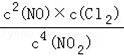
 ,
,
则[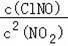
 ]2÷
]2÷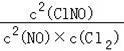
 =
=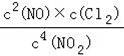
 ,即K=
,即K=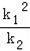
 ,故A正确;
,故A正确;
B.10min时反应达到平衡,测得容器内体系的压强减少20%,则平衡时混合气体总物质的量为(0.2+0.2+0.1)mol×(1﹣20%)=0.4mol,10min内用ClNO(g)表示的平均反应速率v(ClNO)=7.5×10﹣3mol•L•min﹣1,则平衡时n(ClNO)=7.5×10﹣3mol•L•min﹣1×10min×2L=0.15mol,设①中反应的NO2为xmol,②中反应的Cl2为ymol,则:
2NO2(g)+NaCl(s)═NaNO3(s)+ClNO(g)
xmol 0.5xmol
2NO(g)+Cl2(g)═2ClNO(g)
2ymol ymol 2ymol
则0.5x+2y=0.15,(0.2﹣x+0.2﹣2y+0.1﹣y)+0.5x+2y=0.4,联立方程,解得x=0.1、y=0.05,
故平衡后c(Cl2)=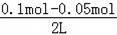
 =2.5×10﹣2mol•L﹣1,故B正确;
=2.5×10﹣2mol•L﹣1,故B正确;
C.平衡常数只受温度影响,其他条件保持不变,反应在恒压条件下进行,则平衡常数K2不变,故C错误;
D.平衡时NO2的转化率为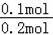
 ×100%=50%,故D正确,
×100%=50%,故D正确,
故选C.
2、将98%(物质的量浓度为18.4mol·L-1)10mL的浓硫酸与等体积的水混合,冷却到室温,下列关于所得溶液的说法正确的是
A.溶质物质的量浓度大于9.2mol/L B.溶液体积为20mL
C.溶质质量分数为49% D.溶质质量分数小于49%
【知识点】物质的量浓度
【答案】
A
3、下列有关平衡常数说法正确的是
A.温度越高,K值越大 B.K值越大,反应的转化率越小
C.K值越大,反应的转化率越大 D.K值的大小与起始浓度有关
【知识点】化学平衡
【答案】












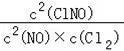
 ,
,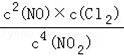
 ;
;