
兴义效果好的音乐生文化课辅导班?
1、 体验还不错老师讲的很容易听懂,师资力量也很好,超多好老师,这次体验真的超级好,环境舒适干净,学习的氛围很浓厚
2、孩子偏科有点严重,数学和地理特别差,就想给孩子找个补习班,看过很多家机构,终选择了新学高考。环境很不错,老师教的也很好,娃娃很喜欢。
3、新学高考一直以来坚持“以人为本、因材施教”的教育理念,帮助高三学生们进行入学前的学能学科测评,在初次诊断中查找学生学习过程中的存在的问题,后面制定出适合学生自身特点的学习方案再进行分班教学。
 兴义效果好的音乐生文化课辅导班
兴义效果好的音乐生文化课辅导班 新学高考艺考生文化课补习班型:
VIP一对一
基础提升班(5)
重难点突破班(9)
新学高考师资介绍
新学高考五年来专注于高考,五年来形成学校自己的教学系统,学校的老师更是从事多年高考的老骨干教师,历年来的教学方法受到广大高考生尤其是艺考生的认可,另外,新学高考每年还会注入具有三年高考从教资格的优秀教师,在这里,学生会感受到不同老师不同的教学方法。
 兴义效果好的音乐生文化课辅导班
兴义效果好的音乐生文化课辅导班习题
1、25℃时,用浓度为0.1000 mol·L-1的NaOH溶液滴定20.00 mL浓度均为0.1000 mol·L-1的三种酸HX、HY、HZ,滴定曲线如下图所示。下列说法正确的是( )
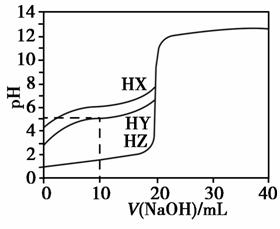
A.在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX
B.根据滴定曲线,可得Ka(HY)≈10-5
C.将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(X-)>c(Y-)>c(OH-)>c(H+)
D.HY与HZ混合,达到平衡时:c(H+)= +c(Z-)+c(OH-)
+c(Z-)+c(OH-)
【知识点】电离平衡单元测试
【答案】
解析:根据中和滴定曲线先判断HX、HY和HZ的酸性强弱,再运用电离平衡、水解平衡知识分析、解决相关问题。
由图像可知,当V(NaOH)=0(即未滴加NaOH)时,等浓度的三种酸溶液的pH大小顺序为HX>HY>HZ,则酸性强弱顺序为HX<HY<HZ,相同条件下三种酸溶液的导电能力顺序为HX<HY<HZ,A项错。当V(NaOH)=10 mL时,HY溶液中c(H+)=10-5mol·L-1,c(OH-)=10-9mol·L-1,c(Na+)=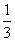 ×0.1000 mol·L-1,据电荷守恒得c(H+)+c(Na+)=c(OH-)+c(Y-),即10-5mol·L-1+
×0.1000 mol·L-1,据电荷守恒得c(H+)+c(Na+)=c(OH-)+c(Y-),即10-5mol·L-1+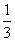 ×0.1000 mol·L-1=10-9mol·L-1+c(Y-),则有c(Y-)≈
×0.1000 mol·L-1=10-9mol·L-1+c(Y-),则有c(Y-)≈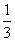 ×0.1000 mol·L-1,c(HY)=
×0.1000 mol·L-1,c(HY)=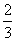 ×0.1000 mol·L-1-
×0.1000 mol·L-1-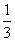 ×0.1000 mol·L-1=
×0.1000 mol·L-1=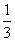 ×0.1000 mol·L-1,那么Ka(HY)=[c(Y-)·c(H+)]/c(HY)=(
×0.1000 mol·L-1,那么Ka(HY)=[c(Y-)·c(H+)]/c(HY)=(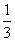 ×0.1000 mol·L-1×10-5mol·L-1)/(
×0.1000 mol·L-1×10-5mol·L-1)/(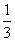 ×0.1000 mol·L-1)=10-5,B项正确。HX的酸性比HY的弱,滴定至HX恰好完全反应时,HY也完全反应,此时溶液中的溶质为NaX和NaY,X-的水解程度比Y-的水解程度大,则有c(Y-)>c(X-),C项错。HY和HZ混合,达到平衡时,据电荷守恒有c(H+)=c(Y-)+c(Z-)+c(OH-);对于弱酸HY来说,Ka(HY)=[c(H+)·c(Y-)]/c(HY),则有c(Y-)=[Ka(HY)·c(HY)]/c(H+),故c(H+)=[Ka(HY)·c(HY)]/c(H+)+c(Z-)+c(OH-),D项错。
×0.1000 mol·L-1)=10-5,B项正确。HX的酸性比HY的弱,滴定至HX恰好完全反应时,HY也完全反应,此时溶液中的溶质为NaX和NaY,X-的水解程度比Y-的水解程度大,则有c(Y-)>c(X-),C项错。HY和HZ混合,达到平衡时,据电荷守恒有c(H+)=c(Y-)+c(Z-)+c(OH-);对于弱酸HY来说,Ka(HY)=[c(H+)·c(Y-)]/c(HY),则有c(Y-)=[Ka(HY)·c(HY)]/c(H+),故c(H+)=[Ka(HY)·c(HY)]/c(H+)+c(Z-)+c(OH-),D项错。
答案:B
点拨:知识:酸碱中和滴定,酸性强弱与溶液导电能力的关系,弱酸电离平衡常数计算,溶液中离子浓度的比较。能力:考查考生的综合分析能力、逻辑推理能力和计算能力。试题难度:较大。
2、下列反应中,属于加成反应的是
A.SO3+H2O=H2SO4
B.CH2=CH2+H2O→CH3-CH2OH
C.CH3Cl+Cl2→CH2Cl2+HCl
D.CO2+2NaOH=Na2CO3+H2O
【知识点】乙烯 烯烃
【答案】
B
3、对Na、Mg、Al的有关性质的叙述正确的是( )
A.碱性:NaOH<Mg(OH)2<Al(OH)3 B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al D.还原性:Na>Mg>Al
【知识点】物质结构 元素周期律单元测试
【答案】
【答案】D
【解析】金属性是Na>Mg>Al,则A.金属性越强,高价氧化物对应水化物的碱性越强,则碱性:NaOH>Mg(OH)2>Al(OH)3,A错误;B.Mg的3s轨道电子处于全充满状态,则第一电离能:Na<Al<Mg,B错误;C.金属性越强,大小越小,则电负性:Na<Mg<Al,C错误;D.还原性:Na>Mg>Al,D正确,答案选D。
考点:考查元素周期律应用




















