
都匀艺体生文化课集训学校推荐?
1、之前在新学高考补习的,就三个月时间提升了快一百分呢,孩子说老师在高考前还会专门开讲座给他们教一些答题技巧,都是干货,孩子能考上大学也要谢谢新学的老师们。
2、 位置还挺好找的,内部环境真的很好。前台妹妹很甜,接待咨询的老师感觉很专业,要先做测评看了测评结果才会沟通课程,意见还是比较中肯的。
3、我想说就是因为学校里的老师管得不严格我才出来补习的吗,我去新学高考补习就是因为那里的管理严格,给我创造了一个舒适的学习环境。
 都匀艺体生文化课集训学校推荐
都匀艺体生文化课集训学校推荐 【新学高考艺考生文化课补习班收费】
不同的学生教学内容和方法及收费各不相同,想要了解费用问题,可以直接电话咨询,由相关负责的老师来解答你的问题。
【专业的师资管理团队】
整合了西南地区知名的教育专家、名校的金牌讲师,教育心理学硕士、高考艺考生补习专家、高考全日制班级金牌管理组、
 都匀艺体生文化课集训学校推荐
都匀艺体生文化课集训学校推荐习题
1、下列说法正确的是()
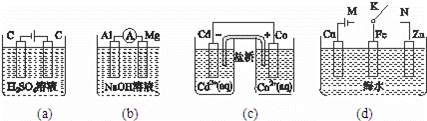
A. 图(a)中,随着电解的进行,溶液中H+的浓度越来越小
B. 图(b)中,Mg电极作电池的负极
C. 图(c)中,发生的反应为Co+Cd2+=Cd+Co2+
D. 图(d)中,K分别与M、N连接时,Fe电极均受到保护
【知识点】电化学 胶体
【答案】
考点: 原电池和电解池的工作原理.
专题: 电化学专题.
分析: A.图a中,实际上为电解水;
B.图b中,铝与氢氧化钠溶液发生反应,铝发生氧化反应,原电池负极发生氧化反应;
C.图c中,负极上失电子,正极上得电子,较活泼的金属为负极,较不活泼的金属为正极,据此写出电池反应式;
D.图d中,K与M连接,连接电源的负极,Fe作阴极被保护,K分别与N连接,形成原电池,Fe为正极被保护.
解答: 解:A.图a中,阳极上氢氧根离子失电子,阴极上氢离子放电,溶液中氢离子浓度增大,故A错误;
B.图b中,铝与氢氧化钠溶液发生反应,铝发生氧化反应,原电池负极发生氧化反应,铝作负极,故B错误,
C.图c中,负极上失电子,发生氧化反应,正极上得电子,发生还原反应,Cd为负极,故金属活泼性Cd>Co,故发生的反应为Cd+Co2+=Co+Cd2+,故C错误;
D.图d中,K与M连接,连接电源的负极,Fe作阴极被保护,K与N连接,形成原电池,Fe为正极被保护,故D正确;
故选D.
点评: 本题综合考查电解池和原电池知识,注意把握电化学工作原理,为2015届高考常见题型,侧重于学生的分析能力的考查,有利于培养学生的良好的科学素养,难度中等.
2、下列对各种平衡体系的叙述中,完全正确的是一组是 ( )
①醋酸溶液中存在的电离平衡:CH3COOH
 CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小;
CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小;
②常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡逆向移动;
③某温度下,容积一定的密闭容器中进行可逆反应:X(g)+Y(g)
 2Z(g)+W(s); △H>0平衡后,升高温度,该化学平衡正向移动;
2Z(g)+W(s); △H>0平衡后,升高温度,该化学平衡正向移动;
④在上述③的可逆反应中,当容器中气体压强不变时,反应达到平衡;
⑤一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡:
CH3COO-+H2O
 CH3COOH+OH-使得溶液中的c(OH-)>c(H+)
CH3COOH+OH-使得溶液中的c(OH-)>c(H+)
⑥在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动
⑦在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
A.①②③④⑤ B.②③④⑤⑥ C.②③⑤⑥⑦ D.①②⑤⑥⑦
【知识点】电离平衡单元测试
【答案】
【答案】C
【解析】①错,加水稀释后,溶液的酸性减弱,PH增大,OH—浓度增大;②正确,醋酸溶液中加入少量的CH3COONa固体使溶液中CH3COO—浓度增大,抑制醋酸的电离,平衡向左移动;③正确,该反应为吸热反应,升高温度平衡向正反应方向移动;④错,该反应为等体积反应,容器内压强为定值;⑤正确,醋酸钠为强碱弱酸盐,溶液显碱性是醋酸根离子水解的结果;⑥正确,加入稀盐酸,溶液中的碳酸根离子浓度减小,溶解平衡将向溶解的方向移动;⑦正确,碘化银的溶解度比氯化银的溶解度小,所以在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀
3、纯碱和小苏打是厨房中两种常见用品,下列区分它们的做法正确的是( )
A.分别用炒锅加热两种样品,全部分解挥发,没有残留物的是小苏打
B.用洁净铁丝蘸取两种样品在煤气灯火焰上灼烧,火焰颜色发生明显变化的是小苏打
C.先将两样品配成溶液,分别加入石灰水,无白色沉淀生成的是小苏打
D.用两只玻璃杯分别加入少量的两种样品,再加入等量的食醋,产生气泡速度快的是小苏打
【知识点】钠的化合物
【答案】
【考点】钠的重要化合物.
【专题】元素及其化合物.
【分析】A.小苏打不稳定,加热易分解;
B.纯碱和小苏打都含有Na元素,焰色反应都呈黄色;
C.纯碱和小苏打都与石灰水反应生成碳酸钙沉淀;
D.碳酸氢钠与醋酸反应较为剧烈.
【解答】解:小苏打的主要成分为NaHCO3,纯碱的主要成分为Na2CO3,
A.小苏打不稳定,加热易分解生成Na2CO3、CO2和水,质量减小,故A错误;
B.纯碱和小苏打都含有Na元素,焰色反应都呈黄色,不能鉴别,故B错误;
C.纯碱和小苏打都与石灰水反应生成碳酸钙沉淀,故C错误;
D.与醋酸反应时,碳酸氢钠产生二氧化碳较快,可直接生成二氧化碳气体,而碳酸钠先与醋酸生成碳酸氢钠,进而继续与盐酸反应生成二氧化碳气体,产生气体较慢,故D正确.
故选D.
【点评】本题综合考查碳酸钠与碳酸氢钠性质的异同,题目难度不大,注意二者与盐酸反应的性质,为易错点,建议写出反应的离子方程式,根据方程式进行判断.












