 福泉音乐生文化课冲刺
福泉音乐生文化课冲刺 福泉音乐生文化课冲刺去哪里好?
1、 课程很满意,这里的老师很负责任,课堂也很丰富有趣,会积极调动孩子,孩子在课堂的参与度也很高,孩子在这里感受到了学习的快乐,并且很乐于配合,孩子很喜欢这里的老师和学习氛围,作为家长很满意这次体验,很不错,值得再来
2、 环境很好,新学高考在成都应该是比较有名气的,本土化里面,做得比较好的一个培训机构了,主要是做中小学文化课培训的。收费说实话很亲民了。师资基本上来说算是不错的。这个校区是其他校区搬过来的,所以老师还是比较好的。总体推荐!
3、孩子学习的事情,一直是我的一件心事,不愿意看到他以后考不上好大学,所以就带他出来补课试试。千挑万选后在新学高考,昨天才收到他班主任给我发的近的学习情况和接下来的安排。
 福泉音乐生文化课冲刺去哪里好
福泉音乐生文化课冲刺去哪里好 【开设班型】
专属VIP:1对1个性化教学 荣耀中班:9到18人班课教学
新学高考管理模式
开展全日制教育,做有价值的教育品牌。
封闭式教学,学生需住在学校为学生安排的学生宿舍
班主任全程管理,学生请假需要向班主任请假方可离校
 福泉音乐生文化课冲刺去哪里好
福泉音乐生文化课冲刺去哪里好福泉音乐生文化课冲刺习题
1、将如图所示实验装置的K闭合,下列判断正确的是( )
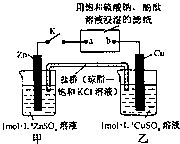
A.Cu电极上发生还原反应
B.电子沿Zn→a→b→Cu 路径流动
C.片刻后甲池中c(SO42﹣)增大
D.片刻后可观察到滤纸b点变红色
【知识点】电化学 胶体
【答案】
【考点】原电池和电解池的工作原理.
【专题】电化学专题.
【分析】A、依据装置图分析装置的K闭合,为原电池装置电解滤纸上的饱和硫酸钠溶液,甲和乙形成原电池反应锌做负极失电子发生氧化反应,铜做正极,电极上得到电子发生还原反应;
B、电子从原电池负极流出经外电路流向电解池阴极a,通过电解质溶液离子定向移动到b;电子不能通过电解质溶液;
C、甲池中锌离子浓度增大,盐桥中的氯离子移向甲池,硫酸根离子浓度基本不变;
D、滤纸处是电解池,a做阴极,氢离子得到电子发生还原反应,水电离平衡破坏附近氢氧根离子浓度增大,酚酞变红,b做阳极氢氧根离子失电子生成氧气,附近氢离子浓度增大;
【解答】解:A,Zn作原电池的负极,Cu作原电池的正极,Cu电极是发生还原反应;故A正确;
B、电子流向是负极到正极,但a→b这一环节是在溶液中导电,是离子导电,电子并没沿此路径流动;故B错误;
C、选项中硫酸根离子浓度基本保持不变;故C错误;
D、选项中是滤纸a点是阴极,氢离子放电,水电离平衡破坏附近氢氧根离子浓度增大,酚酞变红;b做阳极氢氧根离子失电子生成氧气,附近氢离子浓度增大,故D错误;
故选A.
【点评】本题考查电化学知识,原电池、电解池原理的应用,装置图设计有些复杂,B选项干扰作用明显,设问巧妙,题目难度中等.
2、某待测溶液(阳离子为Na+)中可能含有SO42﹣、SO32﹣、NO3﹣、Cl﹣、Br﹣、CO32﹣、HCO3﹣中的一种或多种,进行如图所示的实验,每次实验所加试剂均过量,下列说法不正确的是( )
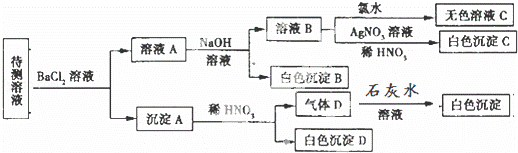
A. SO42﹣、SO32﹣至少含有一种
B. 沉淀B的化学式为BaCO3
C. 肯定存在的阴离子有CO32﹣、HCO3﹣、Cl﹣,还有SO42﹣、SO32﹣至少含有一种
D. 肯定没有的离子是Br﹣
【知识点】离子反应的本质
【答案】
考点: 常见阴离子的检验;常见阳离子的检验.
分析: 待测液和氯化钡溶液反应得到沉淀A,则溶液中可能含有CO32﹣、SO32﹣、SO42﹣,向沉淀中加入稀硝酸生成气体,且有部分沉淀不溶解,则溶液中存在CO32﹣,可能存在SO32﹣、SO42﹣中的两种或一种,根据离子共存知,溶液中不存在Ba2+;
滤液A中有Ba2+,加入过量的NaOH溶液得到白色沉淀B,则溶液中一定含有HCO3﹣,白色沉淀B为BaCO3,滤液B中通入氯气,得无色溶液,溶液中一定没有Br﹣,滤液B中加入硝酸银、硝酸溶液得到白色沉淀,白色沉淀为AgCl,说明滤液B中含有Cl﹣,由于加入氯化钡溶液,不能确定原溶液中是否含有Cl﹣,据此进行解答.
解答: 解:待测液和氯化钡溶液反应得到沉淀A,则溶液中可能含有CO32﹣、SO32﹣、SO42﹣,向沉淀中加入稀硝酸生成气体,且有部分沉淀不溶解,则溶液中存在CO32﹣,可能存在SO32﹣、SO42﹣中的两种或一种,根据离子共存知,溶液中不存在Ba2+;
滤液A中有Ba2+,加入过量的NaOH溶液得到白色沉淀B,则溶液中一定含有HCO3﹣,白色沉淀B为BaCO3,滤液B中通入氯气,得无色溶液,溶液中一定没有Br﹣,滤液B中加入硝酸银、硝酸溶液得到白色沉淀,白色沉淀为AgCl,说明滤液B中含有Cl﹣,由于加入氯化钡溶液,不能确定原溶液中是否含有Cl﹣,
A、根据以上分析可知,待测液中至少存在SO32﹣、SO42﹣中的一种,故A正确;
B、根据分析可知,沉淀B为碳酸氢根离子与钡离子、氢氧根离子反应生成的BaCO3,反应的离子方程式为:HCO3﹣+OH﹣+Ba2+=BaCO3↓+H2O,故B正确;
C、根据分析可知,肯定存在的离子为:CO32﹣、HCO3﹣,不能确定Cl﹣是否存在,故C错误;
D、根据分析可知,待测液中一定不存在的离子为:Br﹣,故D正确,故选C.
点评: 本题考查了常见离子的检验、离子共存的判断等知识,题目难度中等,注意掌握常见离子的化学性质及检验方法,正确分析框图中的转化关系及反应现象是解答本题的关键.
3、分子式 C4H8O2和C5H10O2的两种一元羧酸与乙二醇(HOCH2CH2OH)发生酯化反应,生成分子式为C11H20O4的酯多有(不考虑立体异构)( )
A.6种B.8种C.10种D.12种
【知识点】烃的衍生物单元测试
【答案】
【考点】有机化合物的异构现象.
【分析】分子式C4H8O2的酸有2种:CH3CH2CH2COOH、CH3CH(CH3)COOH,C5H10O2中烷基为﹣C4H9,﹣C4H9异构体有:﹣CH2CH2CH2CH3,﹣CH(CH3)CH2CH3,﹣CH2CH(CH3)CH3,﹣C(CH3)3,故符合条件的有机物的异构体数目为4.据此判断三者形成酯的种类.
【解答】解:分子式C4H8O2的酸有2种:CH3CH2CH2COOH、CH3CH(CH3)COOH,而C5H10O2中烷基为﹣C4H9,﹣C4H9异构体有:﹣CH2CH2CH2CH3,﹣CH(CH3)CH2CH3,﹣CH2CH(CH3)CH3,﹣C(CH3)3,所以C5H10O2的羧酸4种与乙二醇(HOCH2CH2OH)发生酯化反应,生成分子式为C11H20O4的酯多有2×4=8,故选B.













