 贵阳高三文化课辅导
贵阳高三文化课辅导 贵阳高三文化课辅导如何选机构?
1、 超有学习气氛,每一个班级单独的一个教室,讲课也不会影响到隔壁的班级。老师看起来都还比较年轻,平易近人,希望通过学习能让小朋友的学习成绩提高。
2、在去新学高考之前,我们去看了其他几家也是做高考补习的学校,那些学校价格比这里还便宜,后我们还是选择了贵一点的新学高考,我们看中的就是这边的教学服务,就算是贵也是可以接受的。
3、 我是盐道街中学高三毕业生,去年来到新学时上了一节化学老师的课,当时对老师很满意,所以后面一直都跟着老师的节奏走,所以我的化学分数从开始的38分提到了82,感谢京翰所有老师对我的辛苦付出,让我高考取得了一个非常好的成绩,谢谢
 贵阳高三文化课辅导如何选机构
贵阳高三文化课辅导如何选机构 【开设班型】
VIP一对一:针对性教学 18人中班:课堂氛围活跃,有利于同学之间相互交流,促进师生之间的感情。
【新学高考管理模式】
新学高考严格的封闭式管理,安静整洁的教学环境,给学生营造良好的学习氛围,使学生能够静心学习,从而能够有效的提高学习成绩。学生在学校期间,手机、电脑一律由学校统一保管,每周日发放给学生用于与家长联系;可以远离不良性学生的影响,杜绝网瘾。
 贵阳高三文化课辅导如何选机构
贵阳高三文化课辅导如何选机构贵阳高三文化课辅导习题
1、下列卤代烃在KOH醇溶液中加热不反应的是( )
①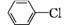 ②
②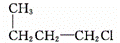 ③(CH3)3C—CHBr2
③(CH3)3C—CHBr2
④CHCl2—CHBr2 ⑤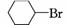 ⑥CH3Cl
⑥CH3Cl
A.①③⑥ B.②③⑤ C.②④ D.全部
【知识点】溴乙烷 卤代烃
【答案】
A
2、下列实验能获得成功的是 ( )
A.乙醇与2mol·L-1的硫酸溶液混合加热到170℃制乙烯
B.苯与溴水反应制取溴苯
C.要鉴别己烯中是否混有少量甲苯,恰当的实验方法是先加足量的酸性高锰酸钾溶液,然后再加入溴水
D.电石与饱和食盐水作用制乙炔
【知识点】有机物的组成 结构和性质
【答案】
D
3、案:D
下列关于粒子结构的描述不正确的是
A.H2S和NH3均是价电子总数为8的极性分子
B.HS-和HCl均是含1个极性键的18电子粒子
C.CH2Cl2和CCl4均是四面体构型的非极性分子
D.SO2和SO3的杂化轨道类型均为sp2,空间构型分别为V形、平面三角形
【知识点】化学键
【答案】
答【答案】C
【解析】
试题分析:A.H2S中H、S元素形成的极性键,但结构不对称,属于极性分子;NH3中含有极性键,空间结构为三角锥形,正负电荷的中心不重合,属于极性分子,故A正确;B.HS-和HCl都只含一个极性键,都具有18个电子,故B正确;C.CH2C12正负电荷的中心不重合,是极性分子,故C错误;D.SO2中S原子形成2个σ键,孤电子对个数=1/2×(6-2×2)=1,价层电子对数为3,为sp2杂化,分子构型为V形,三氧化硫分子中,中心原子硫原子外层6个电子,外围有三个原子,所以不含有孤电子对,价层电子对个数=σ键个数+孤电子对个数=3+1/2(6-3×2)=3,且不含孤电子对,为sp2杂化,三氧化硫分子为平面三角形结构,故D正确,答案为C。
【考点定位】考查极性分子和非极性分子、质子数、中子数、核外电子数及其相互联系。
【名师点晴】根据价层电子对互斥理论确定中心原子杂化类型,价层电子对个数=σ键个数+孤电子对个数,σ键个数=配原子个数,孤电子对个数=1/2×(a-xb),a指中心原子价电子个数,x指配原子个数,b指配原子形成稳定结构需要的电子个数.根据n值判断杂化类型:一般有如下规律:当n=2,sp杂化;n=3,sp2杂化;n=4,sp3杂化;中心原子的杂化类型为sp2,说明该分子中心原子的价层电子对个数是3,无孤电子对数,空间构型是平面三角形;据此判断。











